Dans un DGS-urgent (communiqué envoyé aux professionnels de santé), la Direction générale de santé annonce la disponibilité prochaine du Bamlanivimab, un traitement contre le coronavirus SARS-CoV-2 développé par le laboratoire Eli Lilly. Dans son allocution du 25 février, Olivier Véran a présenté le traitement comme un « nouvel outil » dans l’arsenal pour lutter contre la pandémie de coronavirus. Il est basé sur les anticorps monoclonaux, des anticorps de synthèse. L’ancien président américain Donald Trump a été soigné du Covid-19 en partie avec ce traitement, qui était alors à un stade plus expérimental.
Les anticorps de synthèse sont injectés en intraveineuse et visent la protéine Spike du coronavirus afin d’empêcher le pathogène de se répliquer dans les cellules. Cela revient à reproduire l’action du système immunitaire dans la production d’anticorps, mais plus efficacement et plus rapidement.
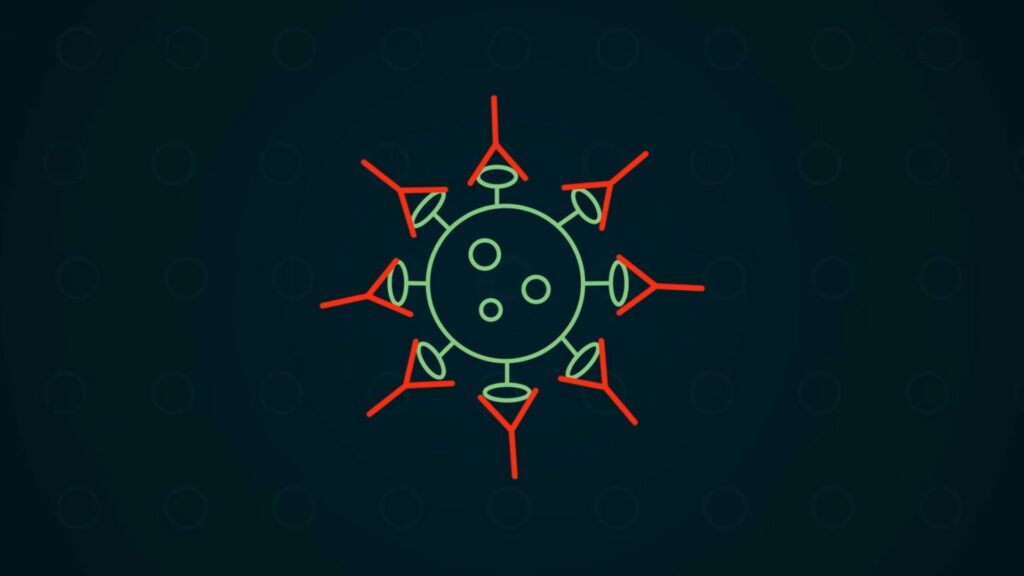
Les anticorps monoclonaux ciblent la protéine Spike du coronavirus SARS-CoV-2.
Source : Louise Audry / Nino Barbey
Selon la DGS, l’administration de ce traitement « pourrait neutraliser le virus à la phase précoce de l’infection ». Le traitement sera donc destiné aux formes légères ou modérées du Covid-19 qui n’ont pas encore entrainé d’hospitalisation. « Pour garantir un maximum d’efficacité, ce traitement doit être initié dans un délai maximal de 5 jours après le début des symptômes », précise le communiqué.
Quels profils ?
Ce traitement basé sur les anticorps monoclonaux sera destiné à certains profils spécifiques de patients — une population cible qui est susceptible d’évoluer par la suite. Seront priorisées les personnes de plus de 80 ans et les personnes de tout âge dont une pathologie entraine un déficit de la réponse immunitaire :
- Chimiothérapie en cours
- Transplantation d’organe solide
- Allogreffe de cellules souches hématopoïétiques
- Maladie rénale avec DFG <30 mL/min ou dialyse
- Lupus systémique ou vascularite avec traitement immunodépresseur
- Traitement par corticoïde >15 mg/semaine
- Traitement immunodépresseur incluant rituximab
- Fibrose pulmonaire idiopathique
- Pathologies rares du foie
- Myopathies avec capacité vitale forcée <70%
- Autres pathologies rares définies par les filières de santé maladies rares (FSMR)
Le parcours patient
Si vous êtes positif au coronavirus, éligible à la population cible de ce traitement, et à un stade précoce de la maladie (5 jours après les premiers symptômes), un document du ministère de la Santé détaille la marche à suivre.
Il faut contacter votre médecin généraliste, ou SOS Médecin au besoin, qui pourra valider ou non l’adéquation de votre profil avec le traitement. Il se peut également que votre médecin constate de lui-même votre éligibilité en vous suivant. Vous serez ensuite orienté vers un lieu d’administration des anticorps monoclonaux — le traitement n’a lieu que dans un environnement hospitalier.
Le traitement prendra la forme d’une perfusion intraveineuse de 700 mg d’une durée de 15 à 60 minutes. Vous resterez en observation une heure pour que les médecins puissent surveiller la survenance d’éventuels effets secondaires, puis, si à l’issue de cette heure rien n’advient, vous pourrez alors rentrer à votre domicile. Le ministère prévient d’ailleurs d’une « possibilité de transport sanitaire pris en charge par la Sécurité sociale ».

Parcours patients lors du soin au Bamlanivimab.
Source : Ministère de la Santé
Les anticorps monoclonaux visent à soigner la maladie. Pendant plusieurs jours, vous serez toujours infecté et, en conséquence, contagieux. Un isolement de 10 jours doit démarrer après le traitement, à l’issue duquel un nouveau test RT-PCR est nécessaire.
C’est une « autorisation temporaire d’utilisation »
Le traitement Bamlanivimab d’Eli Lilly sera autorisé en France à travers une autorisation temporaire d’utilisation (ATU), délivrée par l’Agence nationale de sécurité du médicament et des produits de santé. Il fait l’objet d’un protocole d’utilisation temporaire déjà établi par l’organisme et disponible en ligne.
Cette ATU permet d’autoriser un produit de santé dont les essais cliniques de phase 3 ne sont pas terminés ou publiés, mais dont les résultats de la phase 2 sont aboutis, publiés, et démontrent une nette efficacité en plus d’une sécurité pour les patients. Ce type d’autorisation survient en cas d’urgence — le Bamlanivimab a été récemment autorisé aux États-Unis, et encore auparavant au Canada, via une procédure similaire.
Quelle efficacité pour ce traitement ?
Les essais de phase 2 sont particulièrement positifs. Les résultats, publiés dans The New England Journal of Medicine, montrent une efficacité déterminante pour réduire la charge virale. C’est aussi le cas pour empêcher la survenance des formes graves de la maladie : dans le groupe traité, 1,6 % des patients ont été hospitalisés ; dans le groupe sous placébo, 6,3 % des patients ont vu leur état nécessiter une hospitalisation. La différence est significative.
+ rapide, + pratique, + exclusif
Zéro publicité, fonctions avancées de lecture, articles résumés par l'I.A, contenus exclusifs et plus encore.
Découvrez les nombreux avantages de Numerama+.
Vous avez lu 0 articles sur Numerama ce mois-ci
Tout le monde n'a pas les moyens de payer pour l'information.
C'est pourquoi nous maintenons notre journalisme ouvert à tous.
Mais si vous le pouvez,
voici trois bonnes raisons de soutenir notre travail :
- 1 Numerama+ contribue à offrir une expérience gratuite à tous les lecteurs de Numerama.
- 2 Vous profiterez d'une lecture sans publicité, de nombreuses fonctions avancées de lecture et des contenus exclusifs.
- 3 Aider Numerama dans sa mission : comprendre le présent pour anticiper l'avenir.
Si vous croyez en un web gratuit et à une information de qualité accessible au plus grand nombre, rejoignez Numerama+.
Toute l'actu tech en un clin d'œil
Ajoutez Numerama à votre écran d'accueil et restez connectés au futur !

Pour ne rien manquer de l’actualité, suivez Numerama sur Google !