2019 est l’année internationale du Tableau périodique des éléments. Ce nom résonne sans doute comme un écho à vos cours de chimie du collège ou du lycée : il y a 150 ans, naissait cette classification complexe de tous les éléments chimiques connus.
Le 20 décembre 2018, l’Assemblée générale des Nations Unies a proclamé que l’année suivante serait consacrée à ce référentiel scientifique incontournable, afin d’attirer l’attention sur la manière dont les avancées chimiques peuvent soutenir le développement durable.
D’autres tableaux avant 1869
Vous avez peut-être appris à l’école que l’on doit l’invention du tableau périodique des éléments à un chimiste russe du nom de Dmitri Mendeleïev. En 1869, il publie ses travaux organisant les éléments chimiques en fonction de leur propriétés. Ce modèle doit aussi permettre d’estimer quelles seront les caractéristiques des éléments chimiques restant à découvrir.
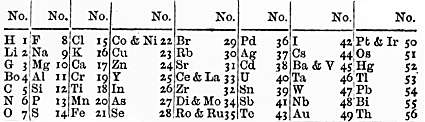
Comme le souligne Mark Lorch, professeur de chimie et de communication scientifique à l’université de Hull (Royaume-Uni) dans un article de The Conversation, d’autres recherches ont pourtant précédées Dmitri Mendeleïev. En octobre 1803, John Dalton — connu pour ses travaux sur le daltonisme — présente un tableau contenant 6 éléments : l’hydrogène, l’azote, le carbone, l’oxygène, le phosphore et le soufre. Ce tableau permettait alors d’établir 13 combinaisons.
Cette trouvaille marque les prémisses de sa théorie atomique, essentielle dans la chimie moderne. Elle change la vision que les contemporains ont de la matière : on l’imaginait à tort décomposable à l’infini, en divisions de plus en plus petites. Grâce à John Dalton, on apprend que la matière est en fait formée par des unités, appelées atomes.
La matière n’est pas décomposable à l’infini
Après lui, un autre chimiste britannique propose sa version du tableau périodique des éléments. En 1863, John Newlands publie un classement des éléments en fonction de leurs masses atomiques. Ce tableau à 7 lignes présente un point faible : il manque des cases vides pour accueillir de nouveaux éléments, alors même que John Newlands avait supposé leur existence.
Des tentatives moquées ou méconnues
Moqué pour ses théories, le chercheur a cependant été l’inspiration directe de Dmitri Mendeleïev. Son propre tableau, publié 5 années après, repose aussi sur la masse atomique des éléments — même si cette nouvelle version est plus complexe.
En Allemagne, le chimiste Lothar Meyer n’obtient guère de reconnaissance. Il a pourtant réussi une étape importante, dès les années 1860 : il parvient à regrouper 28 éléments en 6 familles, en fonction de la configuration électronique. Elle tient elle-même compte de la manière dont les électrons sont distribués dans les atomes. Il faut attendre sa mort à la fin du siècle pour une publication d’une seconde version aboutie.
Le tableau périodique de Mendeleiev, publié en 1869, permet enfin de classer les éléments en respectant leur numéro atomique et en tenant compte de leurs propriétés chimiques. L’une des grandes avancées permises par ce tableau est d’aider à prédire quelles seront les propriétés des éléments restants à découvrir.
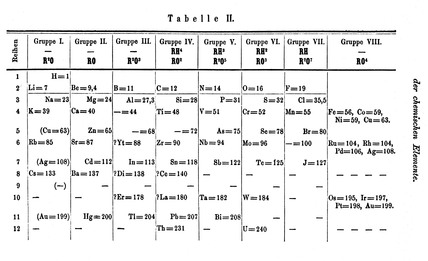
Le tableau périodique des éléments de Mendeleïev (en 1971).
Source : Wikimedia/CC/Science and Society Picture Library, MendeleïevDes ajustements réguliers
L’une des modifications importantes apportée à ce tableau a eu lieu en 1913 : la découverte de l’électron amène le physicien britannique Henry Moseley à classer les éléments en fonction de leur numéro atomique, et non plus en fonction de leur masse. Le nombre d’électrons d’un atome donne son numéro atomique (à condition que l’atome ne soit pas chargé électriquement).
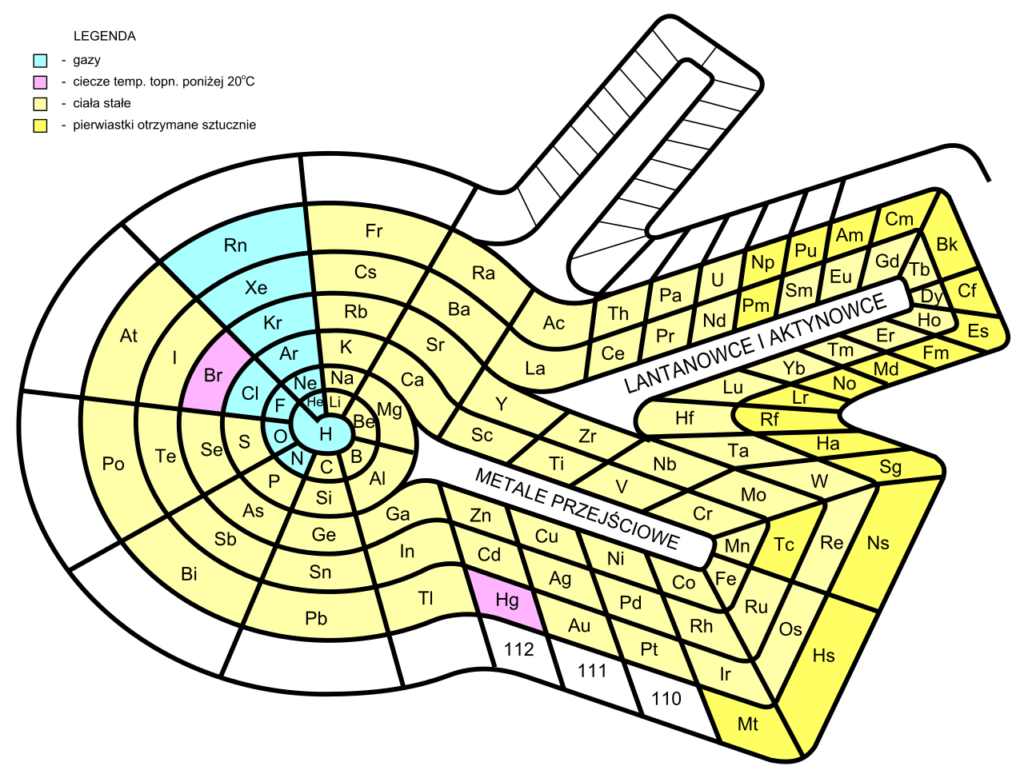
Au cours du 20e siècle, des scientifiques ont tenté de proposer d’autres représentations du tableau périodique des éléments. La plus atypique est probablement celle d’Otto Thedor Benfey, qui eut l’idée de dessiner un tableau périodique étendu en forme d’escargot en 1960.
De nombreux ajustements se sont succédés avant de donner au tableau périodique des éléments la forme que nous lui connaissons actuellement. Sa dernière mise à jour a eu lieu en décembre 2018.
L’union internationale de chimie pure et appliquée a publié son ultime version qui contient 118 éléments, soit presque 100 de plus que dans le tableau de Mendeleïev.
+ rapide, + pratique, + exclusif
Zéro publicité, fonctions avancées de lecture, articles résumés par l'I.A, contenus exclusifs et plus encore.
Découvrez les nombreux avantages de Numerama+.
Vous avez lu 0 articles sur Numerama ce mois-ci
Tout le monde n'a pas les moyens de payer pour l'information.
C'est pourquoi nous maintenons notre journalisme ouvert à tous.
Mais si vous le pouvez,
voici trois bonnes raisons de soutenir notre travail :
- 1 Numerama+ contribue à offrir une expérience gratuite à tous les lecteurs de Numerama.
- 2 Vous profiterez d'une lecture sans publicité, de nombreuses fonctions avancées de lecture et des contenus exclusifs.
- 3 Aider Numerama dans sa mission : comprendre le présent pour anticiper l'avenir.
Si vous croyez en un web gratuit et à une information de qualité accessible au plus grand nombre, rejoignez Numerama+.
Toute l'actu tech en un clin d'œil
Ajoutez Numerama à votre écran d'accueil et restez connectés au futur !

Pour ne rien manquer de l’actualité, suivez Numerama sur Google !