C’est une avancée majeure dans le domaine des biotechnologies. Des chercheurs de l’université de Californie à San Francisco ont créé LOCKR, une protéine totalement artificielle capable de reprogrammer en profondeur les cellules.
Les protéines artificielles ne sont pas une nouveauté en soi. Leur usage est même envisagé pour traiter Alzheimer. Mais là où ces protéines synthétiques provenaient jusqu’ici de molécules naturelles altérées, LOCKR est réellement artificielle, car elle ne trouve aucun équivalent dans la nature.
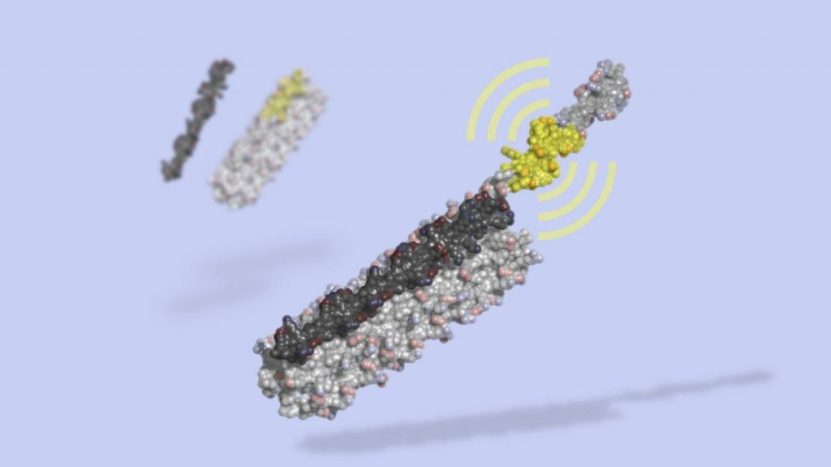
Modélisation de LOCKR.
Source : El Samad
« LOCKR est une biotechnologie qui a été conçue et construite du début à la fin par les humains », explique Hana El-Samad, qui fait partie de l’équipe de recherche. Conçue sur ordinateur puis synthétisée en laboratoire, cette protéine est la première de son genre.
Une protéine sous forme d’interrupteur
Un peu à l’image d’un nanorobot réparateur, LOCKR transforme les cellules normales en cellules « intelligentes ». D’une longueur de 8 nanomètres (0.000008 millimètre), elle est présente directement au sein des cellules vivantes. Dans son état normal, elle est fermée et inactive. Elle a besoin d’une clé : une molécule prévue à cet effet est intégrée par les scientifiques et permet à LOCKR de s’ouvrir.
Une protéine sous forme d’interrupteur, avec des boutons on et off, « procure un niveau sans précédent de contrôle sur la façon dont la protéine interagit avec les autres composants de la cellule », précise Hana El-Samad. Et en effet, une véritable reprogrammation s’opère. La protéine artificielle peut changer l’expression des gènes ; rediriger le réseau cellulaire : dégrader d’autres protéines ; contrôler les interactions entre les protéines.
Une version appelée degronLOCKR a été testée et démontrée sur des cellules humaines cultivées en laboratoire. Dans ce cas précis, les scientifiques ont construit les protéines LOCKR sous forme de circuit biologique autonome, dans le but de dégrader une protéine (réduire le fonctionnement d’une protéine problématique permet de restaurer l’activité normale de la cellule).
Sous forme de circuit, lorsque LOCKR enregistre certains stimuli spécifiques, synonymes d’une anomalie, elle prend alors le contrôle de la cellule. Comme un thermostat automatique, l’action ne se déclenchera que pour le temps nécessaire, avant de se remettre sur « off ».
Des utilités médicales
En utilisant degronLOCKR et des molécules similaires destinées à être développées dans le futur, Hana El-Samad estime dans le communiqué que « nous serons capables de composer des circuits toujours plus sophistiqués, qui pourront très bien conduire à une nouvelle génération de thérapies cellulaires intelligentes, précises et robustes ».
En cas de thérapie cellulaire (pour soigner des organes défaillants), il est parfois difficile pour les médecins de savoir à quel moment précis administrer le médicament biothérapeutique, car il doit intervenir au bon moment et à la bonne dose, sous peine sinon d’être inefficaces voire même d’avoir des effets néfastes.
LOCKR peut non seulement détecter la maladie ou le dommage, mais en plus agir en conséquence au bon endroit, au bon moment et dans des proportions adaptées. La protéine a été littéralement créée pour cet objectif. L’équipe n’hésite pas à envisager que leur invention biotechnologique puisse avoir une application concrète pour aider à soigner des cancers, des tumeurs et des maladies auto-immunes.
« De la même façon que les circuits [électroniques] intégrés ont permis l’explosion de l’industrie des puces informatiques, ces interrupteurs biologiques polyvalents et dynamiques vont bientôt permettre un contrôle précis du comportement des cellules vivantes et, à terme, de notre santé », explique Hana El-Samad dans le communiqué.
+ rapide, + pratique, + exclusif
Zéro publicité, fonctions avancées de lecture, articles résumés par l'I.A, contenus exclusifs et plus encore.
Découvrez les nombreux avantages de Numerama+.
Vous avez lu 0 articles sur Numerama ce mois-ci
Tout le monde n'a pas les moyens de payer pour l'information.
C'est pourquoi nous maintenons notre journalisme ouvert à tous.
Mais si vous le pouvez,
voici trois bonnes raisons de soutenir notre travail :
- 1 Numerama+ contribue à offrir une expérience gratuite à tous les lecteurs de Numerama.
- 2 Vous profiterez d'une lecture sans publicité, de nombreuses fonctions avancées de lecture et des contenus exclusifs.
- 3 Aider Numerama dans sa mission : comprendre le présent pour anticiper l'avenir.
Si vous croyez en un web gratuit et à une information de qualité accessible au plus grand nombre, rejoignez Numerama+.
Toute l'actu tech en un clin d'œil
Ajoutez Numerama à votre écran d'accueil et restez connectés au futur !

Pour ne rien manquer de l’actualité, suivez Numerama sur Google !











