Voilà bien longtemps que la recherche scientifique poursuit l’objectif de percer à jour les mécanismes qui nous font vieillir. En ligne de mire : trouver des « remèdes » de longévité. Même Google travaille à l’immortalité, dans une optique très transhumaniste. Les scientifiques procèdent à leurs recherches essentiellement sur des animaux. C’est le cas pour les travaux dirigés par Jarod A. Rollins, au MDI Biological Laboratory. Dans un article publié dans Cell Reports en juillet 2019, puis dans un communiqué diffusé le 9 janvier 2020, cette équipe révèle avoir augmenté l’espérance de vie chez des vers… jusqu’à 500 %. Et ce par une « simple » modification génétique.
Jarod A. Rollins et ses collègues ont porté leur attention sur le Caenorhabditis elegans. Ce ver rond est souvent le sujet des expériences dédiées à l’augmentation de la longévité. Paradoxalement, si ce nématode intéresse tant la communauté scientifique, c’est du fait de sa très courte durée de vie. Il offre ainsi une version accélérée du vieillissement, montrant un panorama condensé du processus génétique qui va avec. Ce panorama est d’autant plus intéressant que, dans le cadre des expériences, il permet d’assister rapidement aux effets d’un potentiel traitement contre la vieillesse. Ces avantages ont d’autant plus leur importance que le C. elegans a de nombreux gènes en commun avec l’être humain.
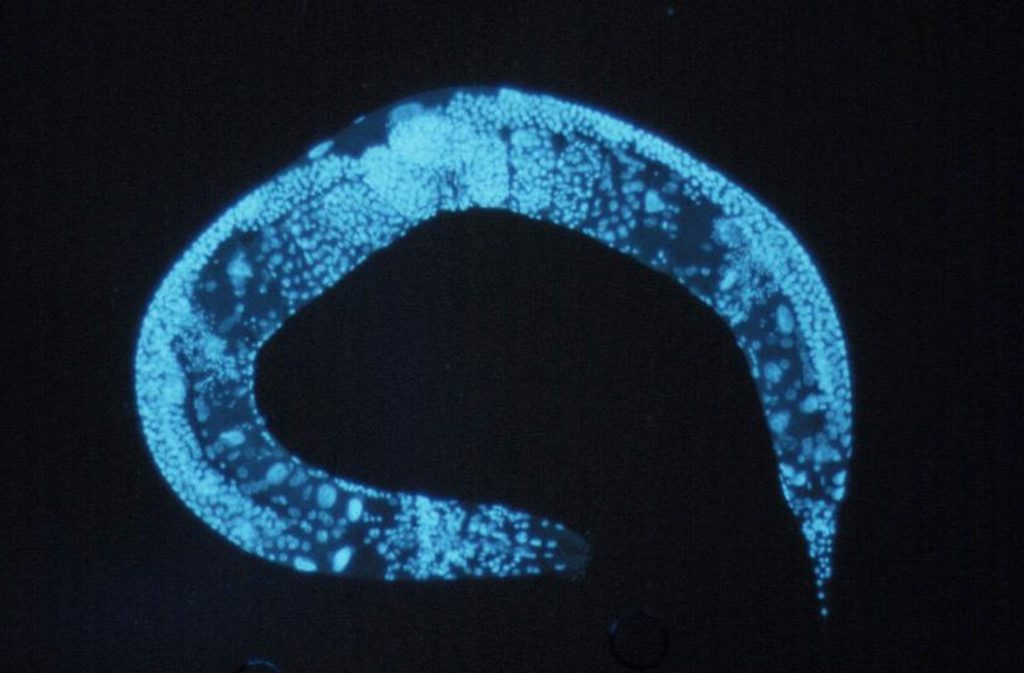
Image au microscope du ver Caenorhabditis elegansn, des vers « ronds ».
Plusieurs « voies cellulaires » ont d’ores et déjà été découvertes chez les vers C. elegans pour augmenter leur longévité. La voie de transduction de l’insuline est la première. Elle est impliquée dans l’homéostasie du glucose, c’est-à-dire dans une bonne régulation du niveau de glucose (le sucre) dans votre corps. L’altération génétique de cette voie cellulaire permet d’augmenter la durée de vie des vers de 100 %. L’autre voie est appelée mTOR et c’est par elle que circule une enzyme régulant la prolifération cellulaire, la croissance cellulaire, la production de protéines par les cellules et même l’expression génétique. Lorsque cette voie est modifiée par les chercheurs, la longévité des vers augmente de 30 %.
Si ces techniques d’augmentation du temps de vie des petits nématodes ont été établies, alors qu’est-ce que Jarod A. Rollins et son équipe ont-ils bien pu découvrir de nouveau ? La réponse se trouve dans un effet fascinant de synergie.
Il n’existe pas de « gènes de l’âge », ce sont des interactions
Les scientifiques ont réussi à coupler les deux précédentes méthodes d’ingénierie génétique que nous venons de citer. Mais ce qui est plus intéressant encore, c’est que le résultat n’est pas une longévité combinée de 130 %. Il ne s’agit pas d’une addition des conséquences des deux altérations. « L’effet n’est pas 1 + 1 est égal à 2, c’est 1 + 1 est égal à 5 », illustrent les auteurs de l’article.
C’est ce phénomène qui relève d’une synergie : la combinaison de facteurs différents génère un effet global plus important, comme un emballement. Finalement, l’espérance de vie chez ces vers a donc augmenté de 500 %, en passant à 3 ou 4 mois, au lieu du temps naturel des 3 à 4 semaines. D’après les estimations des auteurs, une synergie similaire appliquée à des humains porterait notre longévité entre 400 et 500 ans.

Si certaines personnes vivent plus âgée que d'autres, ce n'est probablement pas en raison d'un seul gène ni même d'une catégorie de gènes, mais d'interactions entre plusieurs voies cellulaires, selon cette étude.
Source : PixabayCette découverte met en lumière l’existence d’une interaction cellulaire poussée dans le processus à l’œuvre dans le vieillissement. L’existence d’une synergie pourrait aussi expliquer pourquoi un « gène de l’âge » (ou même une catégorie de gènes) n’a jamais pu être identifié dans des recherches crédibles étudiant la biologie des humains vivant le plus longtemps sur Terre. « Nos résultats démontrent que rien, dans la nature, n’existe dans le vide ; pour développer des traitements plus efficaces contre la vieillesse, nous devons nous intéresser à des réseaux de longévité plutôt qu’à des voies uniques », affirment les chercheurs dans le communiqué.
Les auteurs de l’article précisent qu’ils n’ont pas encore compris la façon dont ces voies cellulaires interagissent. C’est leur prochain objectif, la deuxième étape. « En caractérisant ces interactions, nos scientifiques préparent le terrain pour des thérapies visant à augmenter l’espérance de vie. »
+ rapide, + pratique, + exclusif
Zéro publicité, fonctions avancées de lecture, articles résumés par l'I.A, contenus exclusifs et plus encore.
Découvrez les nombreux avantages de Numerama+.
Vous avez lu 0 articles sur Numerama ce mois-ci
Tout le monde n'a pas les moyens de payer pour l'information.
C'est pourquoi nous maintenons notre journalisme ouvert à tous.
Mais si vous le pouvez,
voici trois bonnes raisons de soutenir notre travail :
- 1 Numerama+ contribue à offrir une expérience gratuite à tous les lecteurs de Numerama.
- 2 Vous profiterez d'une lecture sans publicité, de nombreuses fonctions avancées de lecture et des contenus exclusifs.
- 3 Aider Numerama dans sa mission : comprendre le présent pour anticiper l'avenir.
Si vous croyez en un web gratuit et à une information de qualité accessible au plus grand nombre, rejoignez Numerama+.
Toute l'actu tech en un clin d'œil
Ajoutez Numerama à votre écran d'accueil et restez connectés au futur !

Pour ne rien manquer de l’actualité, suivez Numerama sur Google !













